Gıda ve İlaç Sektörü
Gıda ve İlaçlara İlişkin Denizaşırı İzlenebilirlik Yasaları ve Yönetmelikleri
Genel kalite yönetimi için ISO 9000/9001, gıda için HACCP ve ilaçlar içinse GMP gibi uluslararası kurallara ek olarak, izlenebilirlik işlemiyle ilgili farklı ülke ve bölgelerde kendilerine özgü başka yasa ve yönetmeliklerle de karşılaşmak mümkündür.
Gün geçtikçe küreselleşmenin arttığı bu dönemlerde, izlenebilirliği sağlayabilmek adına denizaşırı yasa ve yönetmelikleri anlamak ve bunlarla ilgili önlemler almak önemlidir. Bu nedenle, bu bölümde AB ülkelerindeki Gıda Yasasının Genel İlkeleri ve ABD’deki Biyoterörizm Yasası gibi çeşitli ülkelerin gıda ve ilaçlarla ilgili yasa ve yönetmelikleri tanıtılmaktadır.
HACCP, Hazard Analysis Critical Control Points (Risk Analizi Kritik Kontrol Noktaları) anlamına gelen bir kısaltmadır. Bu, Birleşmiş Milletler Gıda ve Tarım Örgütü (FAO) ve Dünya Sağlık Örgütü’nün (WHO) ortak bir organizasyonu olan Codex Gıda Komisyonu tarafından 1993 yılında yayınlanan rapora dayalı bir tür gıda hijyeni kontrolü yöntemidir ve dünya genelinde teşvik edilmiştir.
Diğer bir deyişle, HACCP; hammadde kabulünden imalat, işleme ve sevkiyata kadar her aşamada, gıdaların güvenirliği hakkında sorun yaratabilecek gıda zehirlenmesi gibi potansiyel tehlikelerin bilimsel analizlerinin yapılması ve daha sonra bu riski azaltmak veya ortadan kaldırabilmek için gerekli kritik kontrol noktalarının belirlenmesi ile gıda güvenliğini kontrol edebilmek için benimsenmiş bir yöntemdir. Japonya’da HACCP, 1995 yılında başlatılan Kapsamlı Sağlık Hizmetleri Yönetimi ve Üretim Sürecine dahil edilmiştir.
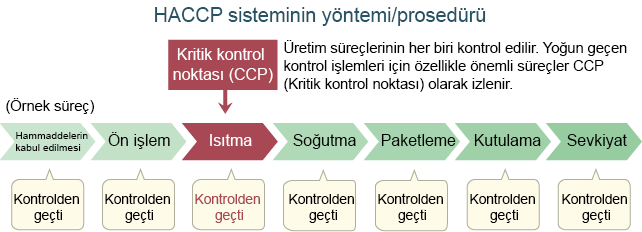
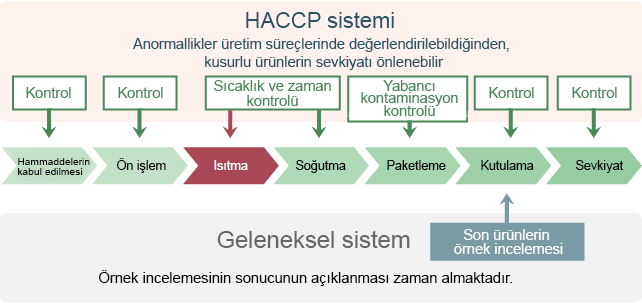
HACCP ile Klasik Hijyen Kontrolü Arasındaki Farklar
Klasik hijyen kontrolü, ilgili tesisler/ekipman ve gıda işleme yöntemleri için standartları belirleyerek ve son ürünleri inceleyerek güvenliği onaylamaktadır. HACCP ise her bir üretim süreci için tehlikeleri analiz eder, önemli süreçlerde daha hassas ve yoğun kontroller yapar ve son olarak her süreç için özel olarak belirlenmiş bir standarda göre kontrol/denetim gerçekleştirir. Süreç boyunca karşı önlemler alındığından, gıda zehirlenmesi ve yabancı atık ve kirletici maddenin girmesi gibi problemler, güvenliği artırabilmek amacıyla, ortaya çıkmadan önlenebilir.
1996 yılında Avrupa’da BSE (deli dana hastalığı) sorunu ortaya çıkmadan önce, AB’nin gıdalara ilişkin birleştirilmiş ve düzenlenmiş ilkeleri yoktu. Bu düzen içerisinde, her madde için ayrı ayrı oluşturulmuş bir yasalar topluluğu kullanılmaktaydı. Bu durum, Gıda Hukukunun Genel İlkeleri (gıda hukukunun genel ilke ve gerekliliklerini belirleyen, Avrupa Gıda Güvenliği Otoritesini kuran ve bu konunun yöntemini belirleyen) birleşik bir yönetmeliğin oluşturulmasına yol açan BSE sorunu ile 2002 yılında yürürlüğe giren gıda güvenliği konuları (EC) No. 178/2002) ön plana çıkmıştır.
İzlenebilirlik Kayıtları için Eşit/Çift Öğeler Belirtilmiştir
İzlenebilirlikle ilgili olarak, Gıda Kanununun Genel İlkeleri Madde 18’de ilkeler şu şekilde tanımlanmıştır: Gıda, yem, gıda üreten hayvanlar ve bir gıdaya dahil edilmesi amaçlanan veya olması beklenen diğer maddelerin izlenebilirliği, yem üretim, işleme ve dağıtımın tüm aşamalarında kurulacaktır.
Gıda tedarik zincirlerinin aşağıdaki bilgileri kontrol otoritelerinin erişebileceği bir durumda saklaması gerektiği belirtilmiştir. Ayrıca, ilkelerin toplamı veya miktar gibi daha ayrıntılı ürün bilgilerinin bir tür tavsiye olarak saklanmasından da bahseder.
ABD’de gıda izlenebilirliği Biyoterörizm Yasası’nda (2002 Halk Sağlığı Güvenliği ve Biyoterörizm Hazırlık ve Müdahale Yasası) belirtilmiştir.
Biyoterörizm Yasası, zorunlu olarak ürünle ilgili tesislerin kaydı, ithalatların önceden bildirilmesi, kayıtların saklanması ve idari gözetim gibi önlemler gerektirmektedir. İzlenebilirlikle ilişkili kanundaki önlemler, kayıtların saklanmasının bir parçasıdır.
Kayıtların saklanması için, ABD’de gıdaların üretim, işleme, paketleme, dağıtım, teslim alma, tutma ve ithalat süreçlerinden hemen önce ve sonra işletmecilerin bu adımları kayıt altına alması ve kayıtların saklanması zorunludur. Daha önceki bölümlerde Tanımlama Sistemi Oluşturma bölümünde açıklandığı gibi, bir adım yukarı ve bir adım aşağı süreçler arasındaki ilişki kanun gereği zorunludur. Ayrıca, bir ürünün insan veya hayvan sağlığını etkileme ihtimali varsa, ilgili işletmeci, kaydı ve ilgili bilgileri Gıda ve İlaç Dairesi’ne (FDA) sunmalıdır.
Kayıt Saklama Süresi
Biyoterörizm Yasası, gıdaların dayanma süresi baz alınarak depolama süresini aşağıda gösterildiği gibi tanımlamıştır:
İlaç yönetim kodu, gıda ve ilaçların güvenliğini sağlayan bir otorite olan Çin Gıda ve İlaç İdaresi (CFDA) tarafından yönetilen ve 2016’dan itibaren kapsamlı olarak çalışmaya başlayan bir sistemdir. Çin’de ilaç satmak isteyen işletmecilerin CFDA’dan onay ve ilaç yönetim kodlarını almaları ve bu bilgileri barkodlar halinde belirtmeleri gerekmektedir.
İlaçların hatalı kullanımını önlemek, takibini sağlamak ve dağıtım verimliliğini artırmak amacıyla 2012 yılında ilaç uygulama yönetmeliği sunulmuştur. Uygulamanın kapsamı şimdiye kadar sınırlı kalmış olsa da 2016 yılından itibaren, denizaşırı işletmeciler de dahil olmak üzere tüm firmaların sistemi uygulaması gerekmiştir. Dolayısıyla, sistemi uygulayacak firmaların, yönetmeliğe uymak adına, tek tek ürünlerin ve ürünlerin ambalajlarının dışına etiket veya işaret yapıştırarak barkodları belirtmeleri zorunludur.

İlaç Yönetim Kodu Yapılandırması
İlaç uygulama kodları 20 digits sayıdan oluşur ve Kod 128C barkodları olarak ifade edilir

| 8 | 123456 | 123456789 | 1234 |
| 1 | 2 | 3 | 4 |
1 Sabit sayı, 1 digit, “8”
2 İdari makamdan (Çin İlaç Elektronik Denetim ve Yönetim Ağı) sağlanan, her bir ürün veya pakete atanan 2 ürün kodu, 6 digits ürün kodu
3 Seri numarası, 9 digits, üreten şirketin üretim için her bir ürününe atadığı numara
4 Doğrulama kodu, 4 digits, doğrulama için veriler








